化學除磷工藝流程講解(污水處理化學除磷)
標簽:
添加時間:2022-10-27 瀏覽次數:1738
全國服務熱線:【152-4428-9576】
1.磷在廢水中存在的形式是什么?
磷是一種活潑元素,在自然界中不以游離狀態存在,而是以含磷有機物、無機磷化合物及還原態這三種狀態存在。污水中含磷化合物可分為有機磷與無機磷兩類。
無機磷幾乎都以各種磷酸鹽形式存在,包括正磷酸鹽、偏磷酸鹽、磷酸氫鹽、磷酸二氫鹽,以及聚合磷酸鹽如焦磷酸鹽、三磷酸鹽等。有機磷大多是有機磷農藥,如樂果、甲基對硫磷、乙基對硫磷、馬拉硫磷等構成,他們大多呈膠體和顆粒狀,不溶于水,易溶于有機溶劑。可溶性有機磷只占30%左右,多以葡萄糖-6-磷酸、2-磷酸-甘油酸及磷肌酸等形式存在。溶解磷占總磷的1/3左右,PO4ˉ-P磷中大分子磷占40%。
2.磷是怎樣轉化的?
水體中的可溶性磷很容易與Ca2+、Fe3+、Al3+等離子生成難溶性沉淀物,例如AIPO4、FePO4等,沉積于水體底部成為底泥。聚積于底泥中的磷的存在形式和數量,一方面決定于污染物輸入和通過地表與地下徑流的排出情況;另一方面決定于水中的磷與底泥中的磷之間的交換情況。沉積物中的磷通過顆粒態磷的懸浮和水流的湍流擴散再度被稀釋到上層水體中,或者當沉積物中的可溶性磷大大超過水體中磷的濃度時,則可能重新釋放到水體中。
3.影響磷存在形式的因素有哪些?
在水中,磷離子以HPO42ˉ還是以H2PO4ˉ形式存在取決于pH值,當pH值在2~7時,水中磷酸鹽離子多數以H2PO4ˉ形式存在,而pH值在7~12時,則水中的磷酸鹽離子多數以HPO42ˉ形式存在。所有含磷化合物都是首先轉化為正磷酸鹽(PO43ˉ)后,再轉化為其他形式。此時測定PO的含量,測定結果即是總磷的含量。
4.磷的來源是什么?
污水中的磷部分來源于化肥和農業廢棄物。同時,生活中含磷洗滌劑的大量使用也使生活污水中磷的含量顯著增加。此外,化工、造紙、橡膠、染料和紡織印染、農藥、焦化、石油化工、發酵、醫藥與醫療及食品等行業排放的廢水常含有有機磷化合物。
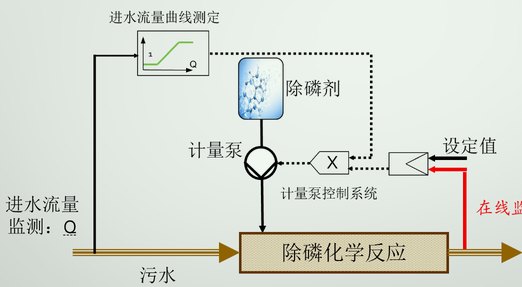
5.化學除磷的概念和工藝是什么?
化學除磷是通過化學沉淀過程完成的,化學沉淀是指通過向污水中投加藥劑,其與污水中溶解性的鹽類,如磷酸鹽混合后,形成顆粒狀、非溶解性的物質,污水中進行的不僅僅是沉淀反應,同時還進行著化學絮凝反應。采用的藥劑一般有鋁鹽、鐵鹽(亞鐵鹽)、石灰、鐵鋁聚合物。
化學沉淀工藝是按沉淀藥劑的投加位置來區分的,實際中常采用的有:前沉淀、同步沉淀和后沉淀。
前沉淀
在沉淀池前投加金屬沉淀劑到原水中。其一般需要設置產生渦流的裝置或者供給能量以滿足混合的需要。相應產生的沉淀產物(大塊狀的絮凝體)則在一次沉淀池中通過沉淀而被分離。如果生物段采用的是生物濾池,則不允許使用Fe2+藥劑,以防止對填料產生危害(產生黃銹)。
前沉淀工藝特別適合于現有污水處理廠的改建(增加化學除磷措施),因為通過這一工藝步驟不僅可以去除磷,而且可以減少生物處理設施的負荷。常用的沉淀藥劑主要是生灰和金屬鹽藥劑。經前沉淀后剩余磷酸鹽的含量為1.5~2.5mg/L,完全能滿足后續生物處理對磷的需要。
同步沉淀
在生物處理過程中投加金屬沉淀劑。同步沉淀是使用最廣泛的化學除磷工藝,其工藝是將沉淀藥劑投加在曝氣池出水或二次沉淀池進水中,個別情況也有將藥劑投加在曝氣池進水或回流污泥渠(管)中。目前很多污水廠都采用同步沉淀,加藥對活性污泥的影響比較小。
后沉淀
將沉淀、絮凝以及被絮凝物質的分離在一個與生物設施相分離的設施中進行,向出水中投加金屬沉淀劑,一般將沉淀藥劑投加到二次沉淀池后的一個混合池中,之后混合沉淀。并在其后設置絮凝池和沉淀池(或氣浮池)。
對于要求不嚴的受納水體,在后沉淀工藝中可采用石灰乳液藥劑,但必須對出水pH值加以控制,比如采用沼氣中的CO2進行中和。采用氣浮池可以比沉淀池更好地去除懸浮物和總磷,但因為需恒定供應空氣而運轉費用較高。
全國服務熱線:【15244289576】
全國服務熱線:【15165428330】


